自2021年9月1日起,我院已启用临床试验管理系统(CTMS),对纸质版资料的接收提出了新的要求,如下
一、 备案资料
备案资料递交仍沿用线下递交形式,递交时间为会议时间往前推两周的周四、周五(择一)(如有特殊情况另行通知)。递交资料前使用微信小程序“快预约”预约递交时间,预约二维码将在院内CRC工作群发送。
二、 审查资料
审查资料需首先登录临床试验管理系统,完成资料上传等流程,秘书形式审查通过后(线上形式审查截止时间为会议时间往前推两周的周三17:00),方可将规定的纸质版资料递交伦理办公室。递交时间为会议时间往前推两周的周四、周五(择一)(如有特殊情况另行通知)。无需预约。
审查资料纸质版递交注意事项:
1)纸质版资料递交时请确保此项目在系统上已通过形式审查,附系统已通过形式审查网页截图。
2)初审资料准备完整的纸质版资料[但英文方案(如有)、IB、CRF需刻在同一光盘中递交,但首尾各2页需纸质版,并盖骑缝章];除初审以外其他类型的审查纸质版资料(例如:修正案、年度/定期跟踪、结题、暂停/终止等)除有PI签字的文件以外,其余全部刻盘。(例如:保留递交信、申请表、方案签字页等此类文件,其余刻盘递交。)
3)递交纸质版资料时请附:线下纸质版递交资料与系统上传资料一致性声明,一致性声明无统一模板,请各研究项目组自拟,申办方盖章。
4)关于本院SAE、方案违背,同样使用系统递交,工作日随时递交纸质版审查资料,需附1)、3)条所需文件。
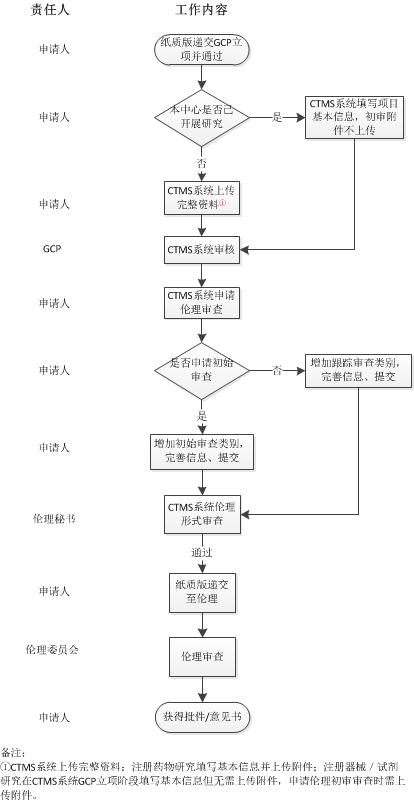
附:注册临床试验审查流程图

Copyright © 2022 浙江省肿瘤医院 ALLRights Reserved 浙ICP备11008795号技术支持:新慧医联
